Au cours des processus physiopathologiques, les cellules sont soumises à une diversité de stress d’origine chimique, physique et biologique. Bien que ces stress diffèrent par leur nature et leur intensité, ils sont généralement intégrés par des réseaux de signalisation moléculaire qui mobilisent des capteurs et effecteurs communs. Cette intégration aboutit à l’activation de programmes adaptatifs complexes visant à restaurer l’homéostasie cellulaire ou, à défaut, à engager des voies alternatives, telles que la sénescence, la plasticité phénotypique ou la mort cellulaire. Ces réponses conditionnent non seulement le devenir individuel de la cellule, mais influencent également l’architecture et la dynamique des tissus environnants. Cette modulation du microenvironnement peut, dans certains contextes, contribuer à la dérégulation des équilibres tissulaires et favoriser l’initiation ou la progression de pathologies inflammatoires chroniques et malignes, menant à des stades cliniquement irréversibles.
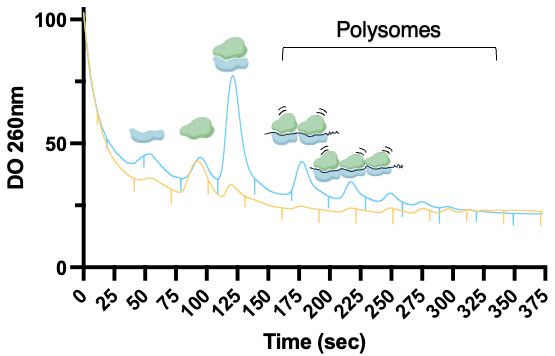
Notre équipe étudie les mécanismes moléculaires détectant et intégrant les signaux de stress microenvironnementaux altérant l’homéostasie des protéines et des ARN. Ces perturbations, intégrées notamment au niveau du ribosome en cours d’élongation, déclenchent des voies de signalisation adaptatives (telles que GCN2 ou la réponse au stress ribotoxique) qui orientent les trajectoires cellulaires et favorisent l’hétérogénéité phénotypique. Nous analysons la dynamique transcriptionnelle et traductionnelle de ces réponses en conditions physiologiques, où elles soutiennent l’homéostasie tissulaire, et pathologiques, où leur dérégulation promeut plasticité adaptative et résistance thérapeutique. Composée de personnels chercheurs et hospitaliers, notre objectif est d’identifier les réseaux adaptatifs et leurs vulnérabilités pour développer des stratégies cliniquement pertinentes limitant la progression des pathologies inflammatoires chroniques et malignes.
Axes de recherche :
- Caractérisation des mécanismes non canoniques de réponse aux dommages de l’ARN et analyse de leur implication en physiopathologie.
- Identification et étude fonctionnelle de modulateurs chimiques ciblant la réponse aux dommages de l’ARN.
Signalisation du stress (stress UV, métabolique, oxydatif et thérapeutique), inflammation, synthese proteique, sénescence, fibrose.

Equipe : Microenvironment stress signaling and epithelial cell fate
Laboratoire de Biologie Tissulaire et Ingénierie thérapeutique
UMR 5305 – Université Claude Bernard Lyon 1 -CNRS
Institut de Biologie et Chimie des Protéines
7, passage du Vercors 69367 LYON CEDEX 07, FRANCE
E-mail : cedric.chaveroux@cnrs.fr


Profils Linkedin :

Profils Research Gate :



